|
Por
lo general existe confusión entre la corrosión electrolítica y la galvánica. La diferencia es simple, mientras que la corrosión
galvánica es causada por una corriente eléctrica generada por dos diferentes materiales en un medio conductor tal como el agua salada, la corrosión electrolítica es causada por una
corriente producida por una fuente externa, por lo general la batería de la embarcación o alguna otra fuente eléctrica.
En un sentido técnico, el termino electrólisis se refiere a la descomposición de una sustancia química producida por el flujo de corriente eléctrica a través de ésta. Esto
significa que inclusive dos materiales similares se pueden convertir tanto en el cátodo como en el ánodo de una celda, en el cuál el ánodo sería el corroído.
|
Pero para comprender mejor el término general de corrosión
electrolítica, primero debemos entender 4 términos por separado: CORROSIÓN, ELECTRÓLISIS, CÁTODO Y ÁNODO.
La CORROSIÓN es el desgaste o deterioro de una pieza de cualquier material por acción electroquímica, que aplicado a metales normalmente
se puede ver como oxidación, donde el oxígeno del entorno se encarga de descomponer la estructura molecular de los metales haciéndolos
frágiles y dándoles ese color rojizo característico a metales como el hierro y acero o un acabado verde oscuro por patina al cobre y sus aleaciones.

|
|
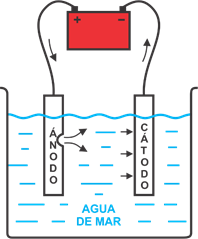
La ELECTRÓLISIS es el medio por el cual se descompone una sustancia química por efecto de una corriente eléctrica debajo de una solución acuosa, en donde actúan dos
factores importantes en este proceso, que son los electrodos: el CÁTODO, que está conectado al polo negativo de la corriente eléctrica y el ÁNODO, que va al polo positivo.
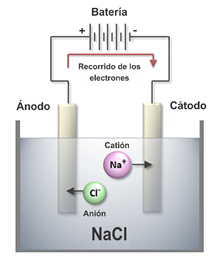
En la electrólisis se ve la descomposición molecular del cátodo atrayendo el ánodo a los iones negativos (aniones) del cátodo y el cátodo atrayendo a los iones positivos del ánodo
(cationes). En esta reacción de óxido-reducción, el ánodo se oxida atrayendo el oxígeno separado del hidrógeno en la solución acuosa mientras el cátodo se reduce.
En el agua salada, la electrólisis no sólo descompone las moléculas de agua, sino todos los minerales que se encuentren en la solución, haciendo que todos los iones positivos de
agua salada, sean recibidos por el ánodo.
|
|
En el casco de un barco, la corriente eléctrica que produce la electrólisis es provocada por errores en el sistema eléctrico de la embarcación y la conductividad del material
del que esté hecho el mismo casco. Las principales causas de corrosión electrolítica son provocadas por fugas de corriente que encuentran tierra en el casco, por ejemplo, una mala
instalación eléctrica, un corto circuito o de una tierra mal aterrizada de alguna herramienta o equipos electrónicos como los sistemas de comunicación, por ejemplo, o bien por derrames
de corriente bajo condiciones de humedad. Un mal cableado en un casco de aluminio, que es altamente conductor de corriente, puede ocasionar el proceso de electrólisis y generar que
piezas como la hélice y la tobera se descompongan por este fenómeno. La única solución para este problema es una buena instalación eléctrica sin fugas, además de tener en cuenta el
nunca utilizar el casco como tierra en el sistema eléctrico.
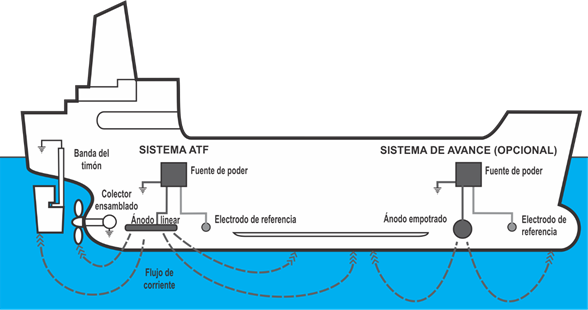
El sistema de cableado deberá estar siempre aislado en el circuito de regreso (dos cables) en lugar de aterrizarlo a tierra. Un switch maestro debe conectarse a la terminal positiva
de la batería y apagarse cuando la embarcación esté en reposo. La toma de tierra (conexión a tierra) es requerida por seguridad cuando existen altos voltajes, por ejemplo, con la
instalación de un generador de 240 volts o la colocación de un puntal abastecedor. En este caso la toma de tierra no deberá de confundirse con la tierra de regreso. La tierra de regreso
siempre lleva corriente mientras que la toma de tierra involucra a un tercer cable que no lleva corriente. Esta toma a tierra se lleva a cabo conectando un cable aislado a una placa de
sacrificio colocada en la parte inferior del casco, lo más alejado posible de las hélices.
Ejemplos de una incorrecta y una correcta conexión a tierra:
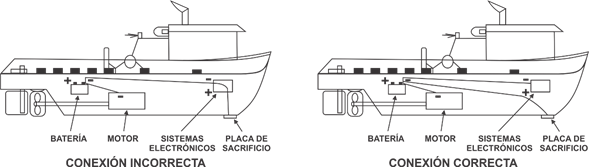
|


